Die Mikroumgebung des Tumors schützt das Krebswachstum
In ihrem Bemühen, Krebs zu bekämpfen, hat die Wissenschaft in den letzten Jahrzehnten begonnen, die Bedeutung der Zellen und Strukturen in der unmittelbaren Umgebung eines Tumors besser zu verstehen. Die Aufklärung des Zusammenspiels zwischen der Mikroumgebung des Tumors und dem Krebs selbst hat auch neue Möglichkeiten für Medikamente zur Überwindung dieser bösartigen Verteidigungszone eröffnet.
Der abnorme Stoffwechsel von Krebszellen beeinflusst die Mikroumgebung des Tumors stark. Die meisten Krebszellen nutzen die aerobe Glykolyse als Hauptenergiequelle und nicht die oxidative Phosphorylierung. Dadurch können sie vermehrt Glukose aufnehmen, die sie als Kohlenstoffquelle für eine schnelle Vermehrung und Metastasierung nutzen.
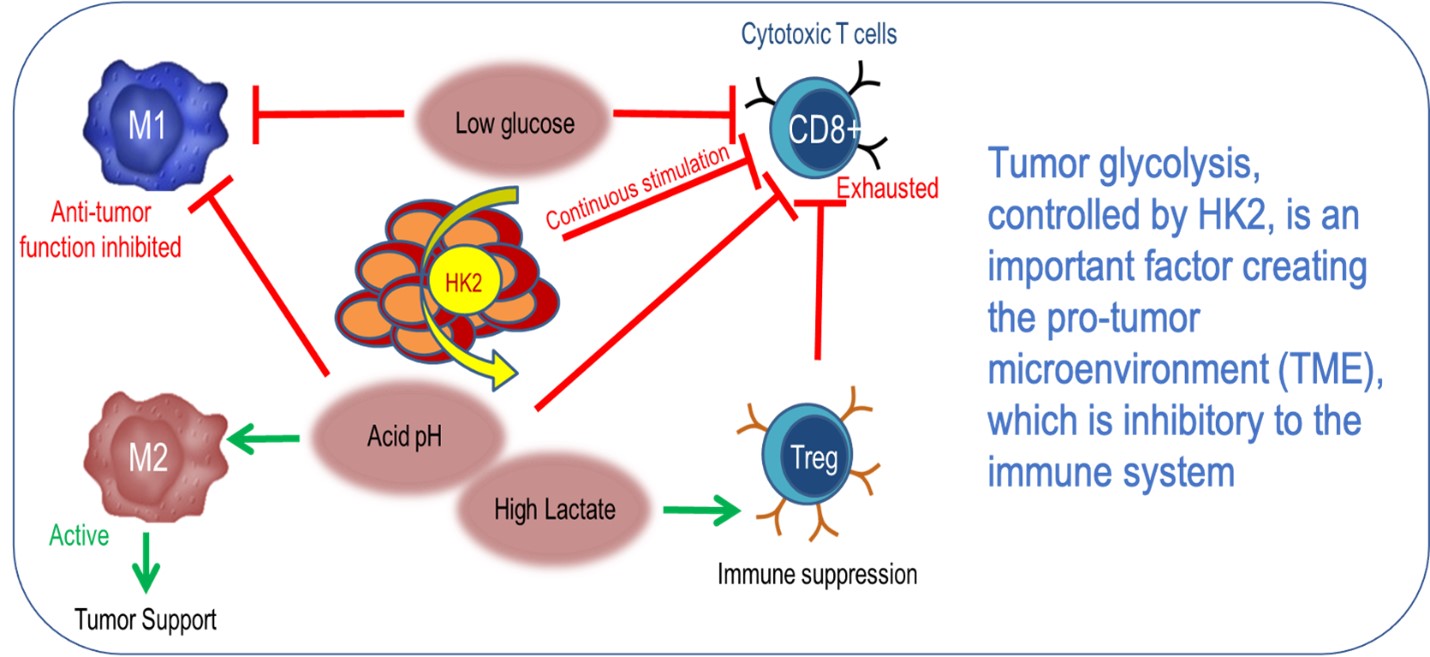
Bei diesem Prozess wandeln die Zellen Glukose in Laktat um - ein Phänomen, das als Warburg-Effekt bekannt ist -, was zu einer sauren und sauerstoffarmen Mikroumgebung führt. Diese veränderte Chemie beeinträchtigt die Wirksamkeit von Therapien wie Bestrahlung oder Chemotherapie, und zwar nicht nur innerhalb der Krebszellen selbst, sondern auch in der Mikroumgebung des Tumors.
Die Wissenschaft ist zwar noch dabei, neue Erkenntnisse über die Mikroumgebung des Tumors zu gewinnen, aber es ist klar, dass diese Festung um den Tumor eine Rolle bei der Unterdrückung des Immunsystems spielt. Erhöhte Laktatwerte fördern das Überleben der Krebszellen, hemmen die Funktion der tumorassoziierten Makrophagen und erleichtern die Immunabwehr der bösartigen Zellen.
Bei erhöhten Laktatwerten neigen die Makrophagen dazu, einen immunsuppressiven Phänotyp anzunehmen, und arbeiten mit den Tumorzellen zusammen, um die Angiogenese, die Bildung von Blutgefäßen zur Versorgung des Tumors mit Sauerstoff, zu fördern. Darüber hinaus unterdrückt Milchsäure die Vermehrung von zytotoxischen T-Lymphozyten um bis zu 95 %.
Wie die auf dem Markt befindlichen Checkpoint-Inhibitoren zeigen, kann eine gezielte Beeinflussung der Mikroumgebung zur Wiederherstellung der Immunreaktion funktionieren. Die überwiegende Mehrheit der Krebserkrankungen spricht jedoch nicht auf diese Therapien an, und es besteht ein Bedarf an neuen Medikamentenklassen, die die schützenden Eigenschaften der Mikroumgebung überwinden. Die neuartigen Arzneimittelkandidaten von Vidac Pharma, die bereits aufregende erste Ergebnisse gezeigt haben, könnten das Versprechen einer bahnbrechenden Lösung in sich tragen.
Der Hauptverursacher - das Hexokinase-2-Protein
Die Arzneimittelkandidaten von Vidac Pharma zielen auf das Enzym Hexokinase (HK) ab, das eine entscheidende Rolle im anormalen Stoffwechsel von Krebszellen spielt. Das Enzym existiert in verschiedenen Isoformen, von denen HK1 und HK2 die häufigsten sind. In normalem erwachsenem Gewebe wird HK1 in großem Umfang exprimiert, um die Glykolyse in harmlosen Situationen wie anaerobem Training zu unterstützen, während die Expression von HK2 begrenzt ist. Im Gegensatz dazu wird HK2 in vielen bösartigen Geweben übermäßig stark exprimiert.
Sowohl HK1 als auch HK2 binden sich an die Mitochondrien - die Kraftwerke der Zelle - über eine Interaktion mit den spannungsabhängigen Anionenkanälen (VDAC), die den Durchfluss vieler Ionen und Stoffwechselprodukte zwischen den Mitochondrien und dem Rest der Zelle steuern. Die mechanische Blockade der Kanäle durch HK2, ein sehr großes Protein, fördert die Glykolyse und damit die Produktion von Laktat, mit allen oben beschriebenen tumorfördernden Folgen. HK2 blockiert auch die Freisetzung von Molekülen, die im gesunden Gewebe den programmierten Zelltod, die Apoptose, auslösen. Dadurch können die bösartigen Zellen ihr Leben verlängern, was für das Gedeihen eines Tumors entscheidend ist.
Entblockierung der Kanäle: der toposterische Effekt
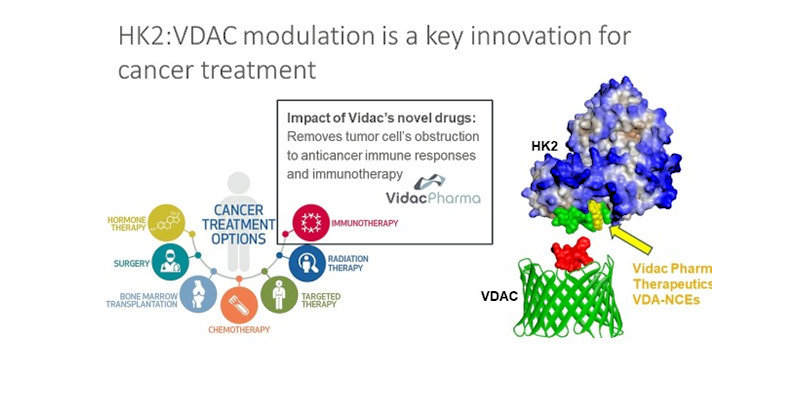
Die Bekämpfung des Warburg-Effekts als zentraler Auslöser von Krebs hat bisher keine medizinischen Ergebnisse erbracht, obwohl das Phänomen seit einem Jahrhundert bekannt ist. Das liegt daran, dass die Glykolyse in gesunden Zellen eine wesentliche Rolle spielt. Würde man die aktive Stelle der HK-Enzyme blockieren, so würde die Glykolyse gänzlich zum Erliegen kommen und die betroffenen Zellen würden absterben.
Vidac Pharma entwickelt ein neues Paradigma, um dieses Problem zu lösen. Mit einer Familie neuartiger chemischer Wirkstoffe, die HK2 daran hindern, die mitochondrialen Kanäle zu blockieren, ohne jedoch seine Funktion als Glykolyse-Katalysator zu unterbrechen, hat das Unternehmen bereits gute Ergebnisse erzielt. Das Unternehmen fand heraus, dass bestimmte natürliche Moleküle - Jasmonate - in der Lage sind, eine Modifikation von HK2 herbeizuführen, die es von seinem VDAC-Anker ablöst, es zurück ins Zytosol schickt und den bösartigen Stoffwechsel der Zelle wieder normalisiert.
Bei Vidac Pharma nennen wir diesen Wirkmechanismus den toposterischen Effekt. Er ist eine Analogie zur allosterischen Regulierung, die stattfindet, wenn Moleküle an bestimmte Stellen eines Enzyms binden, um dessen Aktivität zu steigern oder zu hemmen. Die Vidac-Moleküle binden an eine andere Stelle des Enzyms und verhindern so physisch, dass es sich an die VDAC-Kanäle anlagert.
Der toposterische Effekt ist das neue Paradigma von Vidac Pharma, um Krebs mit Molekülen zu bekämpfen, die dem Rest des Körpers keinen Schaden zufügen. Es hat in vitro und in Phase-2-Tests bei Patienten mit Frühkarzinom und einer lymphatischen Form von Hautkrebs überzeugende erste Ergebnisse gezeigt.

