Vidac Pharma bietet einen bahnbrechenden neuen Wirkmechanismus zur Behandlung von Krebs, der auf ein gemeinsames Merkmal von Krebszellen abzielt, nämlich die Umkehrung ihres abnormalen Stoffwechsels. Vidacs Gruppe neuer chemischer Wirkstoffe stützt sich auf ein dominantes IP-Portfolio mit sieben Patentfamilien. Die Pipeline an neuartigen Therapien bietet Dermatologen, Onkologen und ihren Patienten Wirksamkeit und Verträglichkeit.
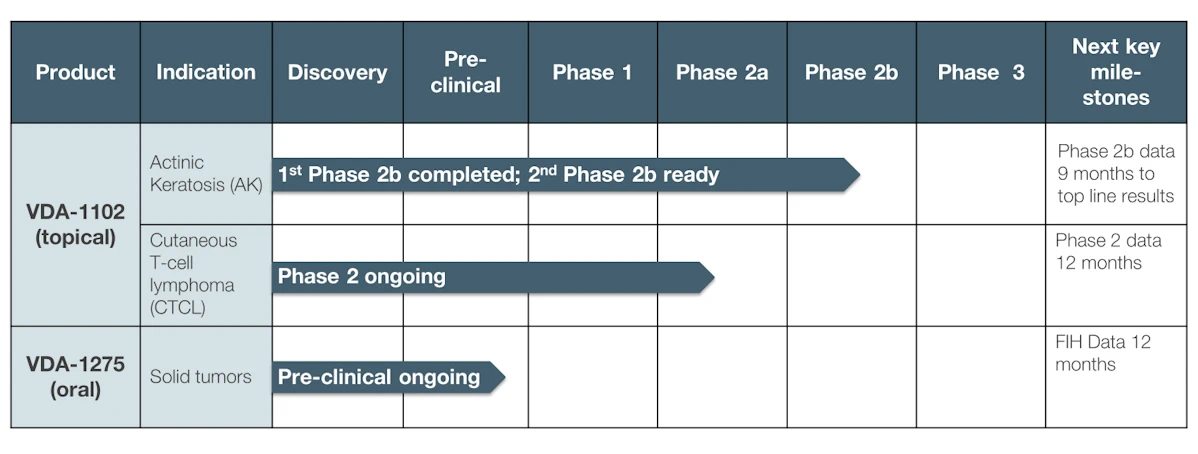
VDA-1102 - Actinic Keratosis (AK)
Die VDA-1102-Salbe ist das erste Medikament aus Vidacs neuer Klasse von Krebsmedikamenten, das selektiv auf bösartige Hautzellen abzielt und nur minimale Auswirkungen auf die umgebende gesunde Haut hat.
Der Wirkstoffkandidat nutzt den neuartigen Wirkmechanismus von Vidac, der den abnormen Stoffwechsel von Krebszellen umkehrt. Die Salbe hat sowohl in In-vitro- als auch in In-vivo-Modellen eine signifikante Wirksamkeit bei aktinischer Keratose (AK) gezeigt, einer frühen Form von Hautkrebs, die sich zu einem Plattenepithelkarzinom der Haut (cSCC ) entwickeln kann.
VDA-1102 ist bei der Verringerung der Läsionen, die sich bei AK entwickeln, ebenso wirksam wie die derzeit auf dem Markt befindlichen Arzneimittel 5-FU und Ingenolmebutat (Picato®). Im Gegensatz zu diesen Behandlungen verursacht VDA-1102 jedoch ein Minimum an unerwünschten Nebenwirkungen, da es auf Tumorzellen und nicht auf gesunde Hautzellen abzielt. Das Medikament verursacht weder eine Nekrose noch eine starke Entzündungsreaktion - Gründe, warum Patienten häufig eine Erstbehandlung vermeiden und eine Wiederholungsbehandlung benötigen - und deckt damit einen erheblichen ungedeckten medizinischen Bedarf.
Zusammenfassung der klinischen Studie:
Eine klinische Phase-2b-Studie bei AK (NCT 03538951), auch bekannt als nicht-melanomaler Hautkrebs, zeigte in einer Post-hoc-Analyse eine 40 %ige vollständige Beseitigung der Läsionen und eine 80 %ige Reduzierung der Läsionen insgesamt. Eine zweite Phase-2b-Studie wird demnächst nur mit Patienten mit fortgeschrittenem AK gestartet, da die frühere Studie bei diesen Patienten eine höhere Empfindlichkeit ergab als bei Patienten mit weniger schweren, z. B. gutartigen Formen der Krankheit. Die Studie wird mit bis zu 40 Patienten in jedem der beiden Studienarme durchgeführt, wobei die Endpunkte die Beseitigung hochgradig proliferativer Läsionen und das Fortschreiten von AK-Läsionen, die sich zu cSCC entwickeln, sind.
VDA-1102 - Cutaneous T-Cell Lymphoma (CTCL)
Die außergewöhnliche Sicherheit, die in Phase 2b für VDA-1102 bei AK festgestellt wurde, ermöglichte es Vidac, direkt in eine Phase-2-Studie für das kutane T-Zell-Lymphom (CTCL), eine Krebsart des Immunsystems, einzusteigen. CTCL wird durch eine Mutation in den T-Zellen verursacht und ist eine seltene Krankheit, bei der Läsionen in der Haut auftreten, bevor sich die Krankheit im Körper ausbreitet. Da es sich bei CTCL um eine seltene Krankheit handelt, kommt es möglicherweise für ein beschleunigtes Zulassungsverfahren in Frage.
Zusammenfassung der klinischen Studie:
Eine Phase-2-Studie ist im Gange. Zwischenergebnisse von 50 % der Probanden im Januar 2024 zeigten günstige Ergebnisse im Vergleich zur Standardtherapie, die eine niedrigere vollständige Ansprechrate und eine viel längere mediane Ansprechzeit aufweist. Dies ist eine offene, Vehikel-kontrollierte Phase-2-Studie zur Bewertung der Wirksamkeit, Sicherheit, Verträglichkeit und Pharmakokinetik der topischen Salbenanwendung von VDA-1102 bei erwachsenen Patienten mit rezidivierter Mycosis Fungoides A im Stadium 1.
[mh1]Die Studie wurde in Israel durchgeführt und hat keine US-FDA-Nummer.
[YS2]Es muss die NCT-Nummer hinzugefügt werden.
VDA-1275, das nächste Mitglied von Vidacs Familie potenter kleiner Moleküle, hat sich in In-vitro-Studien als hochwirksam gegen ein breites Spektrum von Tumorarten erwiesen. Im Februar 2024 gab Vidac außerordentlich gute Ergebnisse für VDA-1275 in verschiedenen Mauskrebs- und menschlichen Zellorganoidmodellen solider Tumore bekannt. Der Medikamentenkandidat zeigte eine statistisch signifikante Wirksamkeit als Monotherapie sowie signifikante synergistische Effekte in Kombination mit zwei Standard-Krebstherapien. Die Studie zeigte auch, dass VDA-1275 selbst eine immunologische Reaktion auslöst. VDA-1275 ist zwar chemisch nicht mit VDA-1102 verwandt, zielt aber auf denselben Wirkmechanismus ab: die Entkopplung der Bindung des Enzyms Hexokinase 2 (HK2) mit den mitochondrialen VDAC-Kanälen.
Zusammenfassung der klinischen Studie:
Das Unternehmen entwickelt VDA-1275 als systemisches Medikament zur Behandlung von soliden Tumoren, wobei der Beginn der First-in-Human-Studien für das erste Quartal 2025 erwartet wird.

